Muchas enfermedades del hígado comparten una característica común: la fibrosis, es decir, la acumulación progresiva de cicatrices en el tejido hepático. Esas cicatrices, que surgen como respuesta del hígado a lesiones o agresiones persistentes, pueden impedir al órgano funcionar correctamente. La fibrosis afecta a millones de personas en todo el mundo y constituye un paso decisivo en la progresión hacia la cirrosis, una patología potencialmente letal que puede evolucionar hacia cáncer de hígado.
Ahora, un estudio del Centro Nacional de Investigaciones Oncológicas (CNIO), publicado en Nature Metabolism, ha identificado un mecanismo clave en el desarrollo de la fibrosis hepática. El hallazgo representa un paso más hacia el desarrollo de terapias personalizadas para evitar su progresión.
Mucho más que simples “tuberías” para la bilis
Nabil Djouder, jefe del Grupo de Factores de Crecimiento, Nutrientes y Cáncer del CNIO, y su equipo han centrado su investigación en los conductos biliares, que atraviesan el hígado transportando la bilis. Más concretamente, en las células que forman esas vías, llamadas células epiteliales biliares (BEC, por sus siglas en inglés).
Hasta ahora, las BEC se consideraban una reserva de células con capacidad para regenerar el hígado. Además de ser los componentes de los conductos biliares, una especie de “tuberías” estancas que transportan la bilis, y le impiden entrar en contacto con el tejido hepático. Este estudio cambia esa visión. Las células BEC no son solo conductos pasivos, sino guardianes activos que regulan el entorno del hígado.
Una estructura que evita el daño hepático
El nuevo estudio del CNIO ha identificado el mecanismo molecular que ayuda a los conductos biliares a evitar la fibrosis. En condiciones normales, las células BEC expresan en su interior una proteína, el receptor FXR. Cuando la bilis circula por los conductos biliares, FXR detecta los ácidos biliares, se une a ellos y activa la producción de otra proteína llamada YAP. Se forman entonces unas moléculas de adhesión que mantienen las células BEC tan pegadas entre sí, que la bilis no tiene acceso al tejido hepático. Al mismo tiempo, YAP limita la proliferación excesiva de células BEC, ya que regula la activación de una tercera proteína esencial para su multiplicación.
Este sistema es clave para que los conductos biliares funcionen como una barrera eficaz. Sin embargo, en algunas enfermedades o condiciones genéticas, la proteína FXR deja de funcionar correctamente o de expresarse, y las células BEC pierden este mecanismo de control: proliferan en exceso, la barrera se debilita y se producen fugas de los ácidos biliares hasta el tejido que realiza las funciones del hígado –el parénquima hepático–.
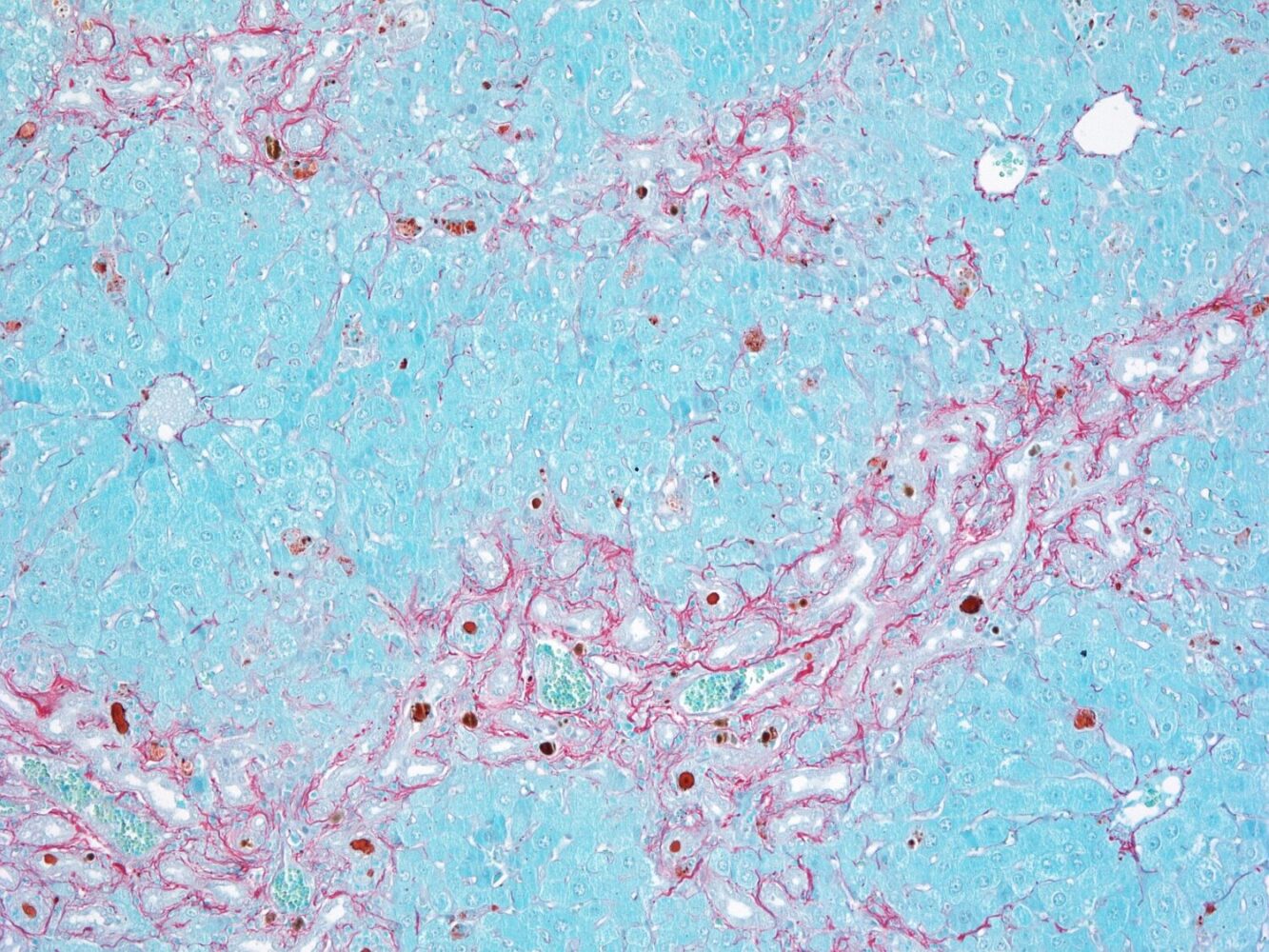
Al llegar a zonas del hígado donde no deberían estar, los ácidos biliares activan otras células –las células estrelladas–, que generan cicatrices. Si estas se acumulan, dan lugar a la fibrosis hepática. Tanto la proliferación excesiva de las células BEC como la fibrosis pueden progresar hacia cirrosis hepática, una enfermedad grave y potencialmente mortal.
Implicaciones clínicas: terapias y estratificación de pacientes
Paula Sánchez, del equipo de Djouder y primera autora del estudio, considera que este trabajo cambia la forma de entender el papel de las vías biliares y subraya la importancia clínica de los resultados: “nuestro trabajo muestra que las células BEC son reguladores activos de la salud del hígado. Al controlar la señalización FXR-YAP, estas células forman una barrera que impide las fugas de ácidos biliares y la fibrosis. Este hallazgo permite encauzar mejor la investigación hacia terapias más seguras y dirigidas”.
Con una combinación de modelos animales –incluido el primer modelo genético de ratón para cirrosis, desarrollado anteriormente por el grupo de Djouder–, análisis computacional y muestras humanas de hígado, el equipo ha demostrado que, cuando se pierden los receptores FXR en las células BEC, la progresión de fibrosis a cirrosis se ve acelerada.
Este conocimiento puede contribuir a establecer cribados para seleccionar a los pacientes para los fármacos dirigidos. Según Djouder, “comprender cómo responden los distintos tipos de células del hígado permitirá seleccionar mejor a los pacientes candidatos a terapias dirigidas a FXR, y evitar posibles efectos adversos en otros pacientes”.
Efecto secundario indeseado de fármacos dirigidos a FXR
Los hallazgos de este trabajo ayudan a explicar los efectos secundarios detectados en un medicamento para enfermedades hepáticas, el ácido obeticólico, u OCA. Este fármaco es un tratamiento de segunda línea –prescrito cuando el tratamiento más habitual no resulta– para enfermedades como la colangitis biliar primaria, que afecta sobre todo a mujeres.
OCA es un ácido biliar semisintético diseñado para activar el receptor FXR con el fin de tratar enfermedades crónicas de hígado que cursan con fibrosis. Sin embargo, en algunos pacientes se ha observado un empeoramiento de la fibrosis tras su administración. Este estudio demuestra que este efecto podría estar relacionado con una disfunción de FXR en las células BEC en estos pacientes, lo que alteraría la respuesta esperada al fármaco.
Djouder destaca que “OCA podría empeorar la fibrosis cuando la señalización de FXR está perdida en las células BEC. Eso explica por qué algunos pacientes pueden experimentar una fibrosis acelerada del hígado, a pesar de estar recibiendo tratamiento”.
Ante estos efectos indeseados la agencia reguladora de medicamentos en Estados Unidos, la FDA, emitió una alerta sobre el uso de OCA, y fue retirado del mercado estadounidense. En Europa, la Agencia Europea del Medicamento recomendó a la Comisión Europea en 2024 revocar la autorización para su venta, pero el Tribunal de Justicia Europeo permitió que se siguiera administrando a los pacientes que ya lo recibían.
Entidades financiadoras
Ministerio de Ciencia Innovación y Universidades (MCIU), también a través de la Agencia Estatal de Investigación (AEI), Unión Europea a través de los Fondos Europeos de Desarrollo Regional (FEDER), Comunidad de Madrid, Asociación Española contra el Cáncer (AECC), Fundación BBVA, Fundación Ramón Areces.
Este trabajo ha sido desarrollado en el CNIO, que está financiado por el Instituto de Salud Carlos III (ISCIII) y el MCIU.
El laboratorio de Nabil Djouder forma parte de la red de excelencia IDIFFER, financiada por el MCIU y la AEI.
Sobre el Centro Nacional de Investigaciones Oncológicas (CNIO)
El Centro Nacional de Investigaciones Oncológicas (CNIO) es un centro público de investigación dependiente del Ministerio de Ciencia, Innovación y Universidades. Es el mayor centro de investigación en cáncer en España y uno de los más importantes en Europa. Integra a medio millar de científicos y científicas, más el personal de apoyo, que trabajan para mejorar la prevención, el diagnóstico y el tratamiento del cáncer.



