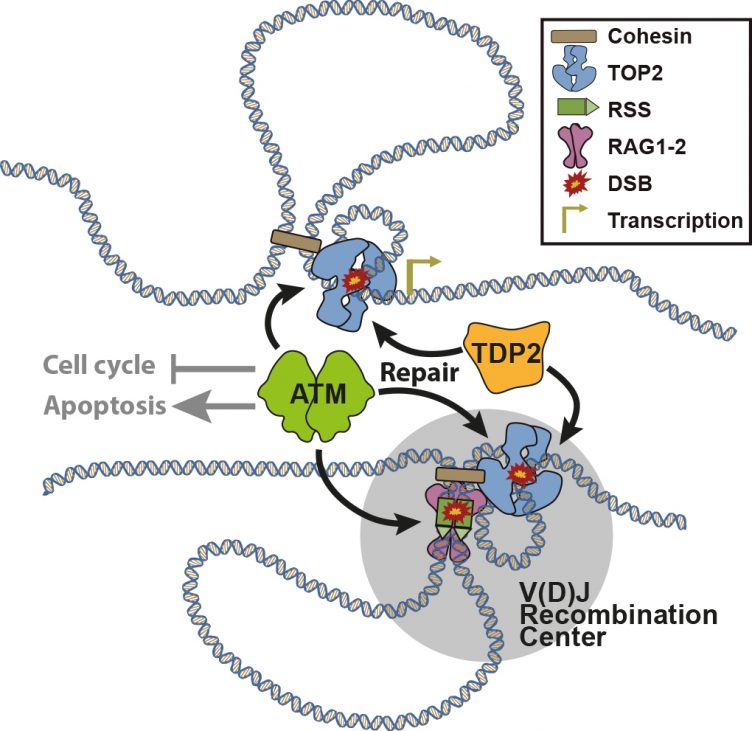
 Modelo para explicar la actividad de la topoisomerasa II como fuente de tumores linfoides deficientes en ATM. /Álvarez-Quilón et al. 2020, Nature Communications
Modelo para explicar la actividad de la topoisomerasa II como fuente de tumores linfoides deficientes en ATM. /Álvarez-Quilón et al. 2020, Nature Communications
Los movimientos y cambios en la estructura tridimensional del material genético producen nudos y enredos en el ADN que, al resolverse, son una fuente de roturas cromosómicas que pueden dar lugar a linfomas, según el estudio publicado en ‘Nature Communications’
Esta investigación abre nuevas vías de estudio sobre los linfomas y el equipo pretende comprobar si estos descubrimientos son extensibles a otros tipos de tumores
Investigadores del Centro Nacional de Investigaciones Oncológicas (CNIO), en Madrid, y del Centro Andaluz de Biología Molecular y Medicina Regenerativa, en Sevilla, han publicado hoy un artículo en Nature Communications que demuestra que losproblemas topológicos en el ADN pueden dar lugar a roturas oncogénicas de forma endógena.
El artículo, titulado ‘Endogenous topoisomerase II-mediated DNA breaks drive thymic cancer predisposition linked to ATM deficiency’, parte de la base de que durante la maduración de linfocitos hay una serie de regiones del genoma que tienen que encontrarse y reorganizarse para que tengan lugar los cambios de secuencia responsables de generar la variabilidad necesaria en la respuesta inmune. “En esta publicación demostramos que estos movimientos y cambios en la estructura tridimensional del material genético producen nudos y enredos en el ADN que, al resolverse, son una fuente de roturas cromosómicas”, afirma Felipe Cortés-Ledesma, investigador principal del trabajo y jefe del Grupo de Topología y Roturas de ADN en el CNIO. “En condiciones en las que la respuesta a estas roturas no es la correcta, aparecen translocaciones cromosómicas que pueden disparar la aparición de linfomas. De hecho, este es el caso de mutaciones en el gen ATM, que son muy frecuentes en tumores hematológicos y responsables del síndrome genético ataxia telangiectasia, que cursa con una elevada predisposición al desarrollo de cáncer de origen linfoide”, añade el investigador.
Este síndrome, la ataxia telangiectasia, también conocida como Síndrome de Louis-Barr, es una enfermedad hereditaria con un patrón de herencia autosómica recesiva que está causada por una mutación en el gen ATM, localizado en el cromosoma 11. De hecho, la Asociación Española Familia Ataxia Telangiectasia (AEFAT) ha financiado parte de trabajo de investigación que hoy se publica y cuyos coautores, aparte de Cortés-Ledesma, son entre otros Alejandro Álvarez-Quilón y José Terrón-Bautista, de Cabimer.
Según explica el abstract del artículo, la quinasa ATM es un regulador maestro de la respuesta a roturas de doble cadena en el ADN y un supresor tumoral bien establecido, cuya pérdida de función es la causa del síndrome neurodegenerativo y propenso al cáncer ataxia telangiectasia. Los pacientes de esta patología están particularmente predispuestos a desarrollar cánceres linfoides. “Nuestros hallazgos demuestran una fuerte relación causal con el desarrollo de cáncer (…), lo que confirma estas lesiones como los principales impulsores de las neoplasias linfoides (…) y potencialmente otras afecciones y tipos de cáncer”, reza en el artículo.
A partir de ahora, esta publicación en Nature Communications abre nuevas vías de investigación relativas al cáncer. Una de ellas, según menciona Cortés-Ledesma, es la posibilidad de “profundizar en los mecanismos moleculares responsables de la aparición y reparación de estas roturas”, así como comprobar si estos descubrimientos son extensibles a otros tipos de tumores. En esta línea, el equipo de investigación apunta la posibilidad de estudios clínicos en pacientes de ataxia telangiectasia.
Dos centros de investigación de excelencia en Biomedicina
En esta investigación colaboran científicos y científicas de dos de los institutos de investigación españoles con mayor trascendencia y trayectoria en biomedicina.
Así, el Centro Nacional de Investigaciones Oncológicas (CNIO)es una institución pública española dedicada a la investigación, diagnóstico y tratamiento del cáncer adscrita al Instituto de Salud Carlos III (Ministerio de Ciencia e Innovación). Situado entre los 10 primeros centros monográficos de investigación del cáncer en el mundo (informe Scimago; Nature Index), el CNIO cubre todo el recorrido de la I+D+i, desde la investigación básica hasta la clínica, para trasladar los resultados de forma rápida y eficiente al Sistema Nacional de Salud y al mercado farmacéutico y biotecnológico (https://www.cnio.es/).
Por su parte, el Centro Andaluz de Biología Molecular y Medicina Regenerativa (CABIMER) constituye un espacio de investigación multidisciplinar en biomedicina pionero en España, ya que integra la investigación básica y aplicada con la finalidad de traducir los resultados de los trabajos científicos en mejoras directas en la salud y en la calidad de vida de los ciudadanos. Se trata de un instituto mixto entre Consejo Superior de Investigaciones Científicas (CSIC), Junta de Andalucía, Universidad de Sevilla (US) y Universidad Pablo de Olavide (UPO) (https://www.cabimer.es/).
Por su parte, AEFAT es una asociación sin ánimo de lucro creada en 2009 y declarada de Utilidad Pública en 2014, que está formada por familiares y personas relacionadas con enfermos de ataxia telangiectasia de diferentes puntos de España. AEFAT pertenece a FEDER (Federación Española de Enfermedades Raras) y FEDAES (Federación de Ataxias de España) (https://www.aefat.es).
Artículo de referencia
Endogenous topoisomerase II-mediated DNA breaks drive thymic cancer predisposition linked to ATM deficiency. Álvarez-Quilón et al (Nature Communications, 2020). DOI: 10.1038/s41467-020-14638-w