Esta web utiliza cookies para que podamos ofrecerte la mejor experiencia de usuario posible. La información de las cookies se almacena en tu navegador y realiza funciones tales como reconocerte cuando vuelves a nuestra web o ayudar a nuestro equipo a comprender qué secciones de la web encuentras más interesantes y útiles.
os investigadores han creado un ratón que presenta telómeros disfuncionales en el hígado y, como consecuencia, desarrolla alteraciones celulares presentes en enfermedades humanas como la hepatitis crónica o la cirrosis
s la primera vez que se demuestra que alteraciones en el funcionamiento de los telómeros inducen cambios en el hígado que son comunes a enfermedades como la hepatitis y la cirrosis, asociadas a un mayor riesgo de cáncer de hígado
l hallazgo sienta las bases para entender el origen molecular de estas enfermedades, e identifica nuevas estrategias terapéuticas para prevenirlas y combatirlas
Los telómeros, regiones de ADN localizadas en los extremos de los cromosomas, protegen el material genético de las células evitando así mutaciones y alteraciones en el ADN que puedan ser fuente de enfermedad. A lo largo de la vida, estas estructuras se van desgastando en un proceso determinado tanto por factores genéticos como ambientales, de forma que alteraciones en su estructura y/o funcionamiento son una de las causas moleculares que subyace a muchas enfermedades asociadas al envejecimiento. Hasta la fecha, su posible papel en la patología hepática como la cirrosis, la hepatitis, o el cáncer de hígado era desconocido.
En un trabajo publicado en la revista Journal of Hepatology, Fabian Beier y Paula Martínez, del Grupo de Telómeros y Telomerasa del Centro Nacional de Investigaciones Oncológicas (CNIO) liderado por Maria Blasco, han creado un modelo de ratón que recapitula el origen de enfermedades humanas asociadas al daño hepático sostenido en el tiempo, o crónico, como la hepatitis o la cirrosis hepática, que a la vez pueden resultar con el tiempo en cáncer de hígado. El nuevo ratón, que presenta telómeros disfuncionales en el hígado, pone de manifiesto la disfunción telomérica como factor desencadenante de estas enfermedades.
Para estudiar la conexión entre daño hepático y los telómeros, los investigadores generaron un ratón deficiente para la proteína TRF1 en el hígado, desprotegiendo así los telómeros de las células hepáticas y comprometiendo su funcionamiento; TRF1 forma parte de un complejo protector de los telómeros denominado shelterina (del inglés, shelter o protección), para proteger el material genético.
Cuando los investigadores sometieron estos ratones deficientes en TRF1 a estrés crónico mediante el agente hepatotóxico CCl4 —causante de toxicidad en el hígado— observaron que las células hepáticas, además de contener múltiples núcleos, presentaban también características propias de los pacientes con cirrosis o hepatitis, como son un incremento en los marcadores de p21, ciclina D1 o PCNA.
“Estos estudios identifican una nueva ruta molecular, la de los telómeros, en el origen de enfermedades hepáticas como la cirrosis, la hepatitis o el cáncer de hígado, así como nuevas estrategias terapéuticas con las que poder prevenirlas y combatirlas”, concluyen los investigadores.
La investigación ha contado con la financiación del Ministerio de Economía y Competitividad, la Fundación Botín, la Unión Europea y la Fundación Lilly.
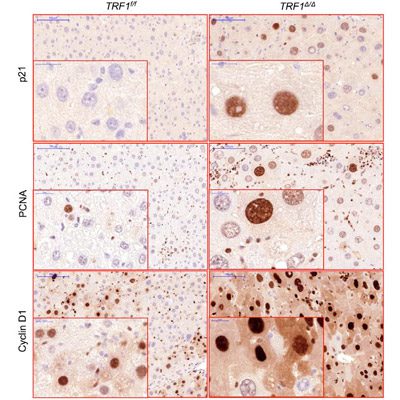
Las células hepáticas sin TRF1 (derecha) presentan, bajo estrés crónico, núcleos más grandes y otros marcadores propios de pacientes con cirrosis o hepatitis (incremento en p21, ciclina D1 y PCNA), en comparación con las células normales sometidas al mismo estímulo (izquierda). /CNIO
Artículo de referencia
Chronic replicative stress induced by CCL4 in TRF1 knockout mice recapitulates the origin of large liver cell changes. Beier F, Martinez P, Blasco MA. J Hepatol. (2015). doi: 10.1016/j.jhep.2015.03.022
