Esta web utiliza cookies para que podamos ofrecerte la mejor experiencia de usuario posible. La información de las cookies se almacena en tu navegador y realiza funciones tales como reconocerte cuando vuelves a nuestra web o ayudar a nuestro equipo a comprender qué secciones de la web encuentras más interesantes y útiles.
Un trabajo muestra cómo la vía PI3K modula la protección de los telómeros al actuar sobre TRF1
La inhibición de PI3K provoca la disminución de los niveles de TRF1 y la desestabilización de los cromosomas
PI3K y AKT –componente de esta vía– emergen como nuevas dianas para atacar a los telómeros
La estructura de proteínas que protegen los telómeros (shelterinas, del inglés “escudo protector”) son prometedoras dianas para combatir el cáncer pero hasta la fecha no hay forma eficaz de atacarlas. En ausencia de fármacos que destruyan los telómeros, el cáncer retiene una de sus propiedades más temibles, la capacidad de sus células de dividirse sin control. Hace dos años, el grupo dirigido por Maria A. Blasco en el Centro Nacional de Investigaciones Oncológicas (CNIO) dio con varios compuestos que provocaban daño en estas estructuras protectoras de los cromosomas y ahora, en un trabajo publicado en Nature Communications, muestran que estas drogas consiguen este efecto al actuar sobre PI3K, una proteína clave en cáncer y en envejecimiento. Se trata de la primera vez que se describe un vínculo funcional entre esta ruta y los telómeros.
 El Grupo de Telómeros y Telomerasa del CNIO lleva años explorando vías para atacar a los telómeros como forma de bloquear la división de las células cancerígenas y causar su muerte. En un trabajo publicado en 2015, describían una nueva estrategia para lograr este objetivo tras el fracaso de los inhibidores de la telomerasa, una enzima que es necesaria para alargar los telómeros pero cuya inhibición no los destruye de manera inmediata.
El Grupo de Telómeros y Telomerasa del CNIO lleva años explorando vías para atacar a los telómeros como forma de bloquear la división de las células cancerígenas y causar su muerte. En un trabajo publicado en 2015, describían una nueva estrategia para lograr este objetivo tras el fracaso de los inhibidores de la telomerasa, una enzima que es necesaria para alargar los telómeros pero cuya inhibición no los destruye de manera inmediata.
“La idea era buscar fármacos que fueran capaces de disminuir los niveles de TRF1, una de las shelterinas esenciales para la integridad de los telómeros”, señala Blasco. “Encontramos varios que al administrarlos inducían daño en estas estructuras y provocaban así que las células cancerígenas no se pudieran dividir, pero no sabíamos cuál era su diana exacta”. Eso es, precisamente, lo que han averiguado ahora.
DESPROTEGER AL TELÓMERO
Blasco, junto a las investigadoras de su grupo Paula Martínez y Marinela Méndez-Pertuz (primeras autoras del trabajo), plantearon la hipótesis de que la disminución de TRF1 se debía a la acción de PI3K, ya que los compuestos utilizados –desarrollados en el CNIO– pertenecen a una serie identificada previamente como inhibidores de PI3K. Esta molécula forma parte de una ruta clave en el envejecimiento (la primera en ser identificada), descrita por Cynthia Kenyon gracias a sus trabajos con C. elegans. Asimismo, PI3K es una de las proteínas más mutadas en cáncer.
Al administrar estos compuestos químicos, los investigadores observaban que los niveles de TRF1 disminuían y, además, la acción de PI3K se inhibía pero no sabían si había una conexión y cuál podría ser. Aquí entra en escena otro de los componentes de la vía PI3K llamado AKT. En condiciones normales, una de las funciones de PI3K es modificar AKT, activándola por fosforilación. Sin embargo, esta reacción no se produce en presencia de los inhibidores de PI3K.

“A continuación estudiamos si AKT modificaba de algún modo a TRF1 y vimos, por medio de distintos experimentos, que efectivamente esto era así –continúa Blasco–; AKT también modificaba a TRF1 fosforilándola”. Al bloquear PI3K, se bloquean estas reacciones de fosforilación y TRF1 pierde estabilidad, tiene una vida media más corta y se une menos al telómero, desprotegiéndolo.
ALIADOS CONTRA EL CÁNCER
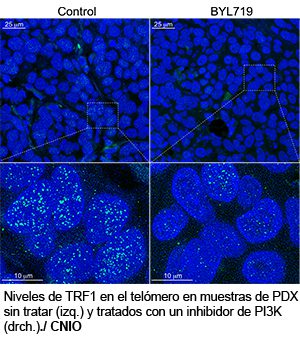
Este hallazgo podría tener implicaciones en el manejo de algunos tumores que presentan mutaciones en PI3K y que se están tratando hoy en día con inhibidores de esta molécula. Blasco y sus colegas han comprobado en ratones Avatar o PDX –en los que se hace crecer un tumor derivado de un paciente para comprobar la eficacia de diferentes terapias– que la respuesta al tratamiento con estos inhibidores de PI3K está relacionada con la disminución en los niveles de TRF1.
A la luz de estos resultados, parece que la actividad antitumoral de los inhibidores PI3K depende de su acción sobre TRF1. Por tanto, cabe pensar que aquellos pacientes que desarrollan resistencia a estos fármacos podrían beneficiarse del tratamiento con otros inhibidores de TRF1. Ése es el siguiente paso.
Este trabajo ha sido financiado por el Ministerio de Economía, Industria y Competitividad (proyecto SAF2013-45111-R), co-financiado por el Fondo Europeo de Desarrollo Regional (FEDER), la Fundación Botín, Banco Santander (División Global Santander Universidades) y Worldwide Cancer Research (WCR 16-1177).
Artículo de referencia
Modulation of telomere protection by the PI3K/AKT pathway. Marinela Méndez-Pertuz, Paula Martínez, Carmen Blanco, Elena Gómez-Casero, Ana Belen García, Jorge Martínez-Torrecuadrada, Marta Palafox, Javier Cortés, Violeta Serra, Joaquin Pastor and Maria A. Blasco (Nature Communications 2017). DOI: 10.1038/s41467-017-01329-2
