Esta web utiliza cookies para que podamos ofrecerte la mejor experiencia de usuario posible. La información de las cookies se almacena en tu navegador y realiza funciones tales como reconocerte cuando vuelves a nuestra web o ayudar a nuestro equipo a comprender qué secciones de la web encuentras más interesantes y útiles.
COLUMNA
Estimados/as Amigos/as:
En los últimos meses hemos realizado nuevos descubrimientos que confiamos ayudarán a avanzar en el diagnóstico y tratamiento del cáncer y de otras enfermedades, y sobre los que podéis leer en la sección de Noticias científicas de este boletín. Pero, además, hemos realizado dos importantes actividades relacionadas con la iniciativa Amigos/as del CNIO, que, como sabéis, está enfocada al 100% a apoyar la investigación del CNIO a través de la contratación de nuevo personal investigador al centro.
El 23 de junio celebramos la Jornada Amigos/as del CNIO, destinada a reconocer vuestro apoyo, el de todos los Amigos y Amigas del CNIO. Este año contamos con la participación de Edurne Pasaban, primera mujer en conseguir culminar los 14 ochomiles del planeta, y quien siempre nos ha apoyado. Así mismo, los investigadores e investigadoras contratadas gracias a Amigos/as del CNIO, nos contaron los avances de sus proyectos de investigación.
Durante el mes de julio celebramos la cuarta edición de CNIO Arte, que siempre hacemos coincidir con la feria de arte contemporáneo ARCO (enlace a la presentación). Este año ha sido muy especial, ya que, gracias a la generosidad de ARCO, hemos disfrutado de un stand propio en la feria, donde se han expuesto todas las obras que se han generado en el contexto de CNIO Arte hasta ahora. Incluida la obra de este año, del artista visual Daniel Canogar, quien se ha inspirado en el trabajo de big data de la vida a través de conversaciones con la investigadora Sarah Teichmann del Wellcome Sanger Institute del Reino Unido. La obra de Daniel Canogar, cuyo título es “Fulguraciones”, fue expuesta en el hall del CNIO desde el 11 de junio hasta principios de julio para que pudieran admirarla los científicos y científicas del CNIO, y posteriormente se trasladó a ARCO durante la semana de la feria para volver a ser expuesta en el CNIO, donde estará de nuevo hasta septiembre.
En el contexto de CNIO Arte, celebramos el segundo Simposio de Arte y Ciencia del CNIO titulado “Cartografiar en la era digital”, que ha servido de foro de reflexión sobre cómo las grandes cantidades de datos que viajan por la sociedad digital están reconfigurando la identidad humana.
El proyecto de CNIO Arte no hubiera sido posible sin la colaboración de la Fundación Banco Santander y la Embajada Británica, a los que quiero dar mis más sinceros agradecimientos por su apoyo al proyecto.
Durante estos meses hemos lanzado 8 nuevos contratos para investigar el cáncer gracias a la solidaridad de nuestros donantes. Gracias a vosotros, que sumáis ya más de 2.000 amigos, el CNIO ha recaudado 2,4 millones de euros durante los seis años de trayectoria de la comunidad de Amigos/as del CNIO. Las donaciones van íntegramente al Programa Internacional de Contratos Amigos/as del CNIO, dirigido a retener talento investigador para abrir líneas de investigación contra el cáncer novedosas sobre metástasis, cáncer infantil o tumores renales y hepáticos, entre otras.
También me gustaría hacer mención a la colaboración pionera en España que hemos establecido con la Fundación Franz Weber, que pasa a formar parte de nuestros Amigos/as del CNIO para impulsar el desarrollo de proyectos de investigación de excelencia que empleen técnicas alternativas a la experimentación animal. Con este acuerdo el CNIO quiere mostrar su más firme apoyo a las buenas prácticas en la experimentación animal, que incluyen la sustitución de animales de experimentación por métodos alternativos.
Nos sentimos muy orgullosos de los logros científicos del CNIO y espero que disfrutéis la lectura de este boletín. Una vez más, muchas gracias por vuestro apoyo, os deseo que paséis un feliz verano.
Maria A. Blasco
Directora
CONOCE A LOS INVESTIGADORES AMIGOS/AS DEL CNIO
Sergio Muñoz
 Sergio Muñoz. /A.Tabernero. CNIO
Sergio Muñoz. /A.Tabernero. CNIO
“Gracias a los Amigos del CNIO por sus generosas donaciones para apoyar esta iniciativa, posibilitando así desarrollar mi trabajo en el estudio de replicación del ADN y la inestabilidad genómica”. Hoy destacamos el trabajo de Sergio Muñoz, que se unió al laboratorio de Juan Méndez dentro del Grupo de Replicación de ADN para desarrollar un proyecto que permita entender cómo el copiado erróneo de nuestro material genético provoca inestabilidad genómica, un fenómeno que se asocia a menudo a varios tipos de cáncer.
Sergio realizó su doctorado aquí, en el CNIO, y después continuó su formación postdoctoral en la Universidad de Sevilla. Volvió al CNIO para trabajar en los mecanismos que producen inestabilidad genómica principalmente porque en el centro hay muchos grupos que trabajan en esta área y, por lo tanto, el CNIO proporciona un entorno excelente para colaborar y trabajar conjuntamente en este tipo de investigación oncológica.
Cuando Sergio estudiaba ciencia básica durante sus estudios universitarios, se dio cuenta de que son muchos los procesos celulares fundamentales que contribuyen al desarrollo del cáncer cuando estos fallan. Decidió así que quería trabajar en investigación oncológica, ya que «todo el mundo conoce a alguien que ha sufrido un cáncer y ésta es una buena forma de ayudar a la sociedad empleando sus aptitudes».
“En el proyecto en el que estoy trabajando, contamos con un sistema que estudia la reduplicación inapropiada de las células cancerígenas. Nos centramos en unos 60 genes relacionados con la replicación y los eliminamos uno a uno para observar si se previene o se empeora la reduplicación, al mismo tiempo que observamos cómo se puede crear una barrera física en el ADN para limitar este fenómeno. Se trata de un proyecto emocionante y estoy encantado de estar de vuelta en el CNIO”.
Nosotros también estamos muy contentos de contar de nuevo con Sergio Muñoz en el CNIO. ¡Gracias a nuestros Amigos del CNIO por facilitar el trabajo de Sergio!
NOTICIAS CIENTÍFICAS CNIO
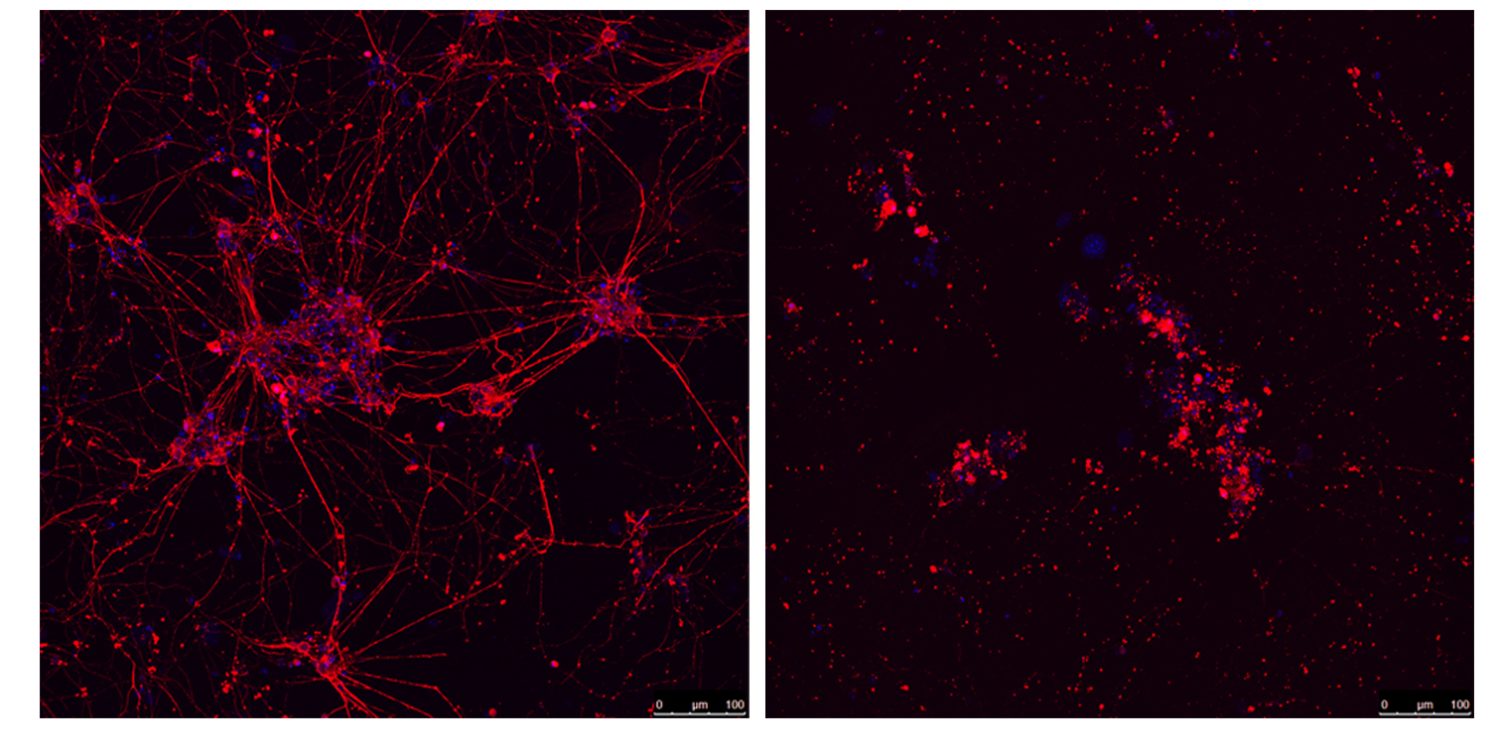 Neuronas motoras de ratón, expuestas (derecha) o no (izquierda) a los péptidos asociados a la ELA (derecha). Tal y como se observa en los pacientes, los péptidos son tóxicos y provocan la muerte de las neuronas. /CNIO
Neuronas motoras de ratón, expuestas (derecha) o no (izquierda) a los péptidos asociados a la ELA (derecha). Tal y como se observa en los pacientes, los péptidos son tóxicos y provocan la muerte de las neuronas. /CNIO
El equipo liderado por Óscar Fernández-Capetillo descubre la causa de la muerte neuronal de gran parte de los pacientes con ELA familiar, una enfermedad que provoca la paralización de los músculos del cuerpo y cuya causa se desconoce. Los investigadores atribuyen esta pérdida a un nuevo mecanismo que bloquea las reacciones celulares que usan ácidos nucleicos (ADN o ARN), lo que impide multitud de procesos fundamentales para el funcionamiento de las células.
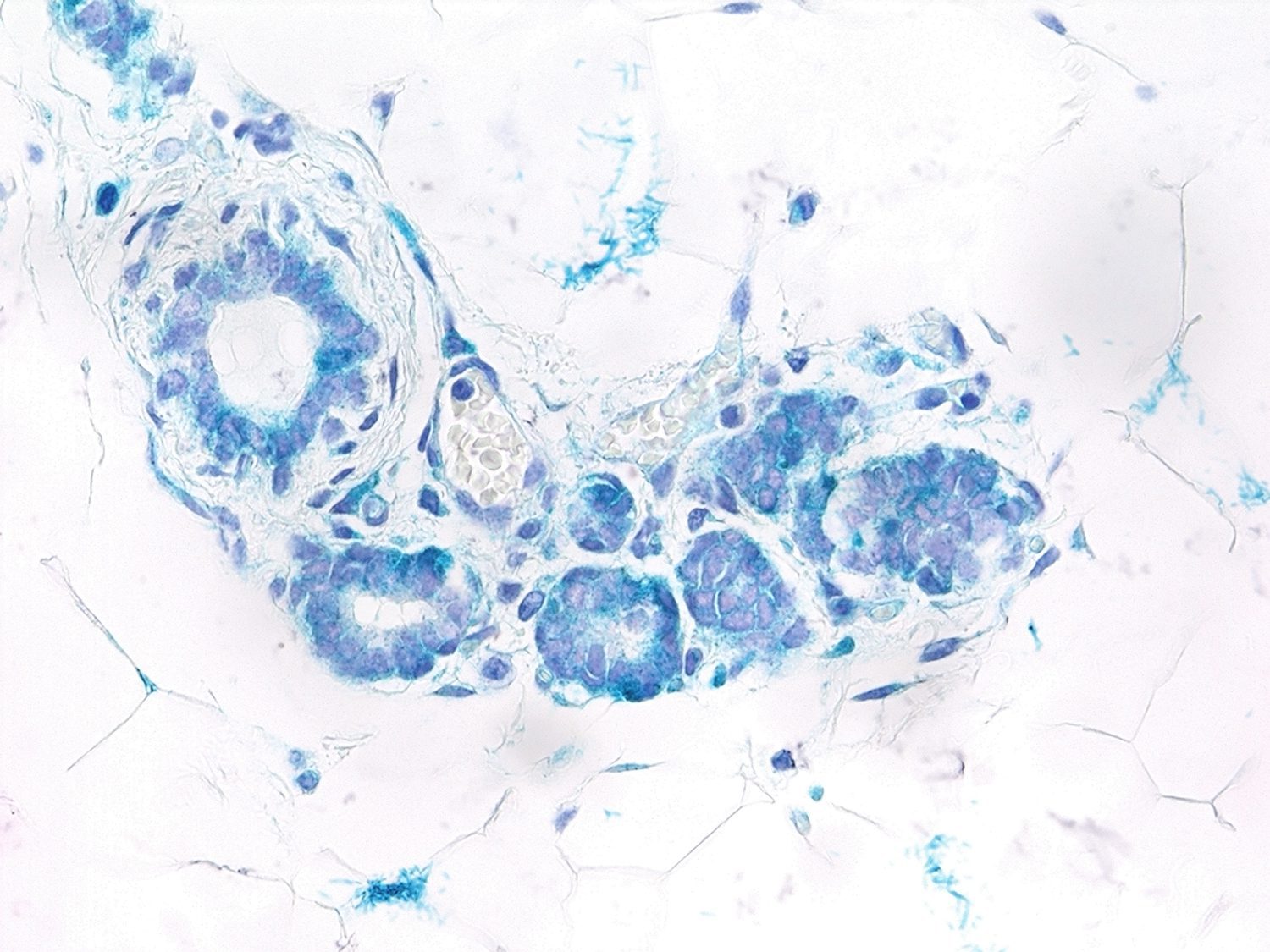 Células epiteliales senescentes (cian) en la glándula mamaria de un ratón con altos niveles de expresión de Rank. La senescencia inducida por Rank es esencial para la expansión de células madre y, aunque inicialmente se traduce en un retraso en el crecimiento tumoral, finalmente promueve la progresión del tumor y la metástasis. /CNIO
Células epiteliales senescentes (cian) en la glándula mamaria de un ratón con altos niveles de expresión de Rank. La senescencia inducida por Rank es esencial para la expansión de células madre y, aunque inicialmente se traduce en un retraso en el crecimiento tumoral, finalmente promueve la progresión del tumor y la metástasis. /CNIO
La investigadora Eva González-Suárez y su equipo han encontrado que una activación excesiva de una señal celular específica asociada al cáncer de mama, la vía de RANK, provoca en las células mamarias una doble función: en las fases más iniciales del cáncer activa la senescencia, que tiene un efecto protector y retrasa la aparición de los tumores; en las fases más avanzadas esta senescencia promueve el crecimiento del tumor, a pesar del engañoso retraso inicial. Actualmente hay en marcha inhibidores contra esta proteína para frenar la agresividad de estos tumores.
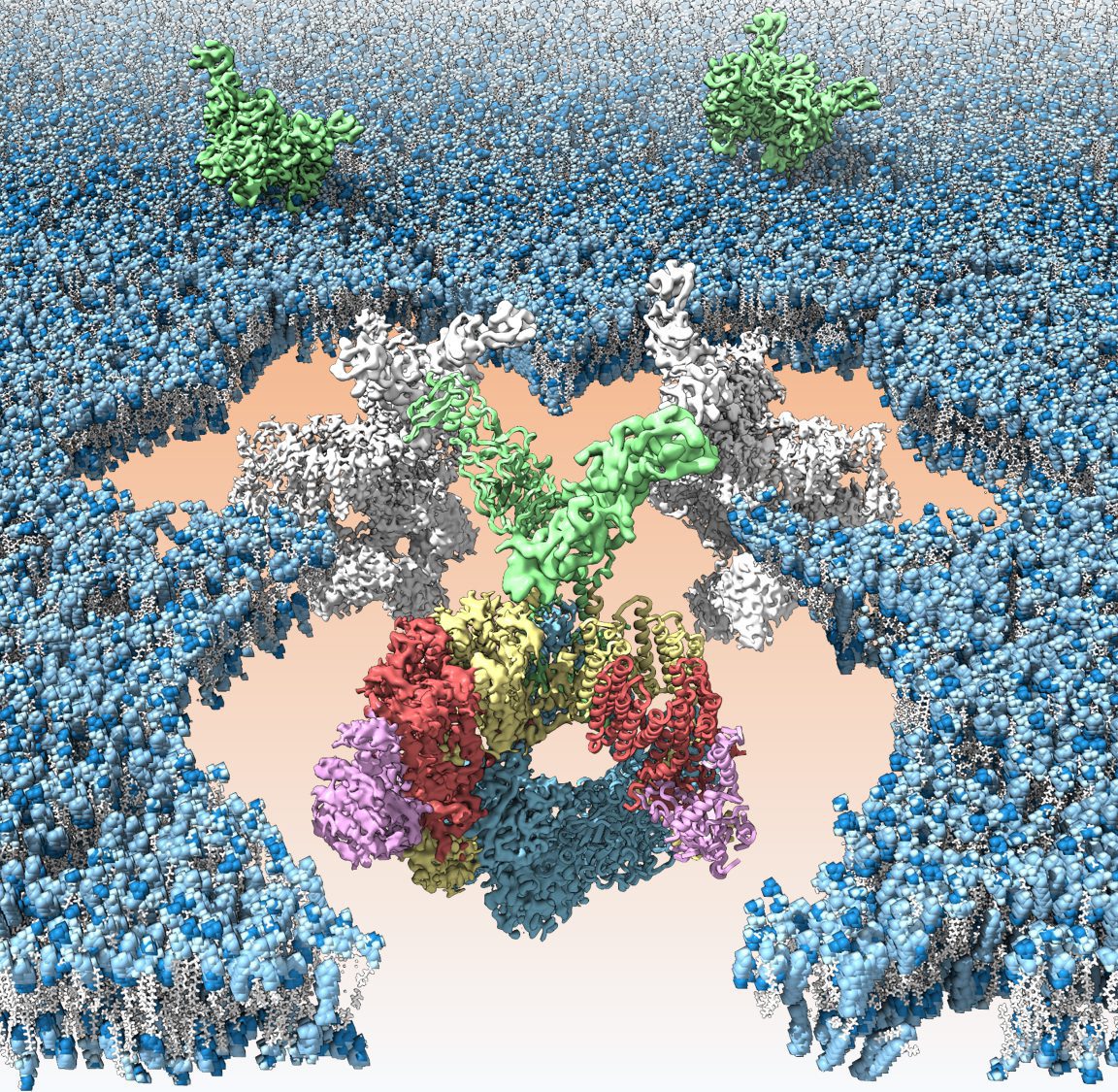 Representación artística del subcomplejo que constituye el sistema de secreción T7SS de 'M. tuberculosis' embebido en la membrana de las células. /CNIO
Representación artística del subcomplejo que constituye el sistema de secreción T7SS de 'M. tuberculosis' embebido en la membrana de las células. /CNIO
La tuberculosis es una enfermedad infecciosa causada por Mycobacterium tuberculosis, una bacteria que afecta habitualmente a los pulmones. Está considerada como la enfermedad infecciosa más mortal de la historia, y todavía, a día de hoy, está entre las 10 más mortales del mundo. Los equipos de Óscar Llorca en el CNIO y Sebastian Geibel en la Universidad de Würzburg (Alemania) hacen una revisión sobre los últimos avances sobre el sistema que permite a la bacteria transportar y expulsar los factores de virulencia para la infección. Con este conocimiento, el objetivo último es poder diseñar moléculas que bloqueen la infección.
 El investigador que ha dirigido el estudio Juan Méndez, en el centro, junto a las investigadoras Elena Blanco-Romero, a la izquierda y Patricia Ubieto-Capella, a la derecha. /A.Tabernero. CNIO
El investigador que ha dirigido el estudio Juan Méndez, en el centro, junto a las investigadoras Elena Blanco-Romero, a la izquierda y Patricia Ubieto-Capella, a la derecha. /A.Tabernero. CNIO
El grupo dirigido por el investigador Juan Méndez ha descubierto que la proteína PrimPol, que facilita la reparación del ADN, podría ser usada para potenciar la quimioterapia. El equipo busca ahora bloquear esta proteína para que las células tumorales sean más vulnerables a los tratamientos oncológicos y mejorar así la eficiencia de la quimioterapia.
 De izquierda a derecha: Ana Belén-Plata Gómez, Alejo Efeyan y Nerea Deleyto-Seldas. /A.Tabernero. CNIO
De izquierda a derecha: Ana Belén-Plata Gómez, Alejo Efeyan y Nerea Deleyto-Seldas. /A.Tabernero. CNIO
El cuerpo humano está adaptado evolutivamente a periodos cíclicos de ayuno o de escasez de nutrientes. El grupo de investigación liderado por Alejo Efeyan descubre que la activación de la proteína RagA es clave en esta adaptación. Los científicos plantean la posibilidad de bloquear estas señales para simular el ayuno en las células sin las dificultades asociadas a la limitación de la ingesta.
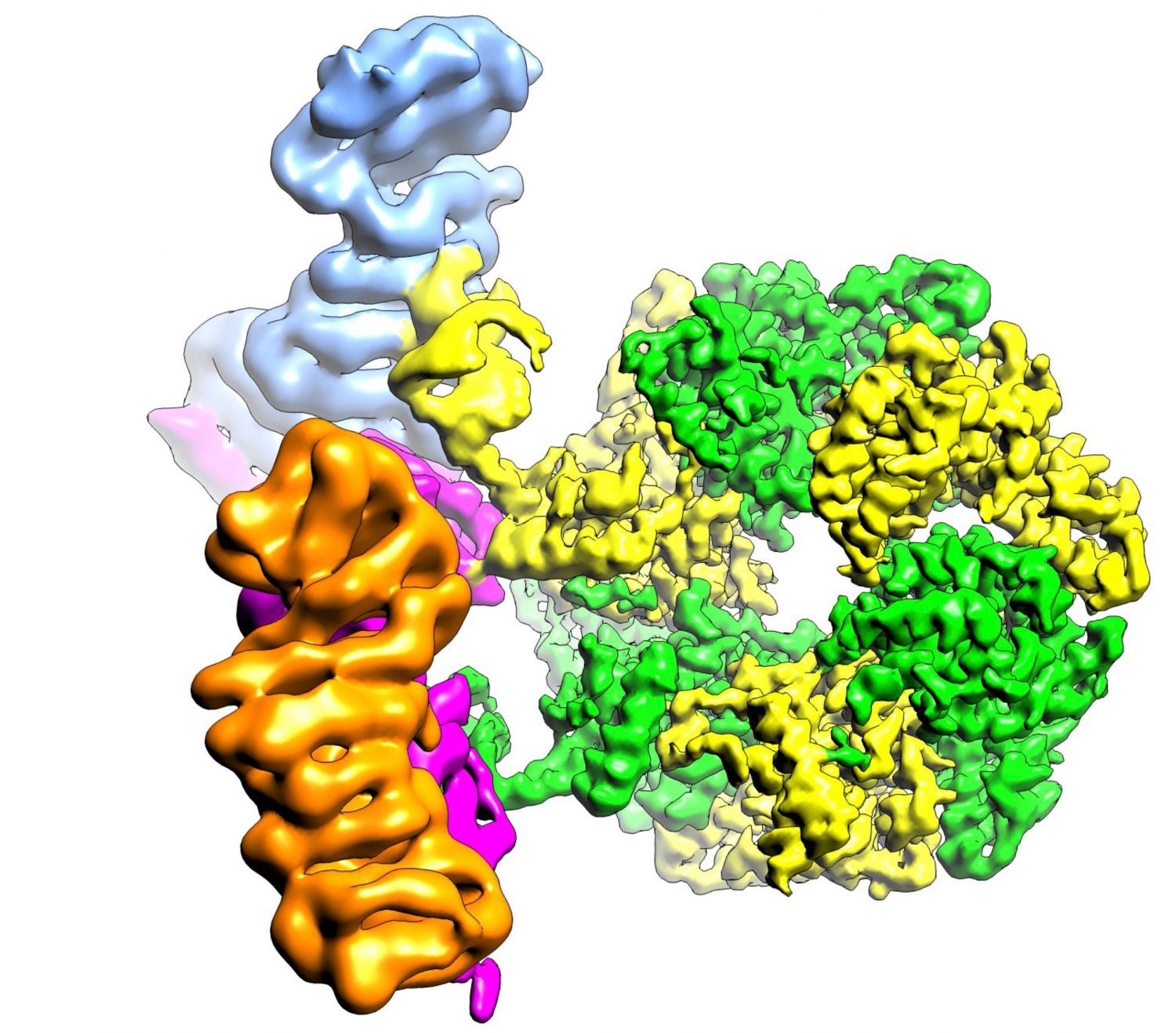 Estructura de las proteínas descifradas en el artículo, unidas al resto de las que forman parte del complejo encargado de ensamblar mTOR. /CNIO
Estructura de las proteínas descifradas en el artículo, unidas al resto de las que forman parte del complejo encargado de ensamblar mTOR. /CNIO
Al menos el 60% de los tumores muestra alguna alteración en la proteína mTOR o en proteínas que interactúan con ella. El equipo de Óscar Llorca ha descubierto la forma en detalle atómico de proteínas que interaccionan mTOR, lo que será fundamental para entender cómo funcionan estas nanomáquinas y diseñar nuevos tratamientos contra el cáncer.
 Alejo Efeyan, jefe del Grupo de Metabolismo y Señalización Celular del CNIO, y Ana Ortega-Molina, primera autora del estudio. /A.Tabernero. CNIO
Alejo Efeyan, jefe del Grupo de Metabolismo y Señalización Celular del CNIO, y Ana Ortega-Molina, primera autora del estudio. /A.Tabernero. CNIO
El equipo coordinado por Alejo Efeyan ha demostrado en modelos animnales que el bloqueo de las señales controladas por la proteína RagC retrasa la aparición del linfoma folicular sin efecto secundarios. Esta estrategia podría ser efectiva también en el tratamiento de enfermedades autoinmunes. Los investigadores buscan ahora inhibidores que sean capaces de bloquear estas señales en pacientes.
 Tumor pulmonar inducido por KRAS4A. /CNIO
Tumor pulmonar inducido por KRAS4A. /CNIO
Desde hace ya casi cuatro décadas se sabe que los oncogenes KRAS son responsables de la cuarta parte de todos los tumores humanos, incluidos algunos de los más malignos como los de pulmón y páncreas. Lamentablamente, no existen fármacos realmente eficaces contra estos tumores, con la posible excepción de Sotorasib, recientemente aprobado. Un trabajo del Grupo de Oncología Experimental liderado por Mariano Barbacid demuestra que las dos proteínas producidas por KRAS pueden producir cáncer y, por lo tanto, solo serán efectivos aquellos tratamientos dirigidos contra sus dos variantes.
NUESTRO CENTRO
Aparte de la celebración de la jornada anual de Amigos/as del CNIO, el evento de CNIO Arte y el lanzamiento de 8 nuevos contratos gracias a las donaciones de nuestros Amigos/as, queremos destacar otros temas importantes relacionados con nuestro centro.
Por un lado, la concesión de las prestigiosas Becas Leonardo a nuestros investigadores Alejo Efeyan y Héctor Peinado, con una cuantía de 40.000 euros cada una. Y, por otro, también queremos destacar la participación del CNIO en las XV Jornadas Internacionales de Ciencia Diverciencia de Algeciras. Esta edición 2021, que se ha realizado en formato telemático debido a la pandemia, ha contado con más de 90 estands, entre los que se encontraba el del CNIO, y más de 32.000 visitas, 10.000 más que el año anterior.
Finalmente, una de nuestras científicas, Marisol Soengas, Jefa del Grupo de Melanoma y Decana para Asuntos Científicos del CNIO, fue nombrada el pasado 13 de julio como Académica Correspondiente de la Real Academia Nacional de Farmacia (RANF). El acto, celebrado por zoom, fue presentado por Antonio Ramón Martínez Fernández, Secretario y Académico de Número de la misma. El nombramiento de Marisol Soengas como Académica de la RANF se suma a los de otros dos científicos del CNIO, Mariano Barbacid y Maria A. Blasco, que fueron nombrados Académicos en 2011 y 2013, respectivamente.
ENTREVISTA
Eva González Suárez
 Eva González Suárez. /A.Garrido. CNIO
Eva González Suárez. /A.Garrido. CNIO
Eva González Suárez lidera el Grupo de Transformación y Metástasis en el CNIO.
¿Cuál es tu meta en relación a la metástasis?
La investigación que realizamos en mi laboratorio va encaminada a identificar nuevos tratamientos que mejoren la supervivencia en tumores epiteliales, principalmente de mama, que está asociada a la metástasis. En la mayor parte de estos tumores, la mortalidad es debida principalmente a la metástasis, ya que el tumor primario se elimina fácilmente en la cirugía. Necesitamos entender mejor la metástasis, y para ello la fisiología del tejido sano, ya que las células tumorales,no inventan nada nuevo, sino que utilizan los mismos mecanismos que las células sanas pero de una forma aberrante.
Uno de vuestros objetivos es verificar si los inhibidores de la vía de RANKL podrían ser eficaces también para prevenir los tumores de mama. ¿Qué indicios tenéis de que esto pueda funcionar?
Los resultados en prevención son muy claros en todos los modelos animales donde se ha testado, así como en células de mama humanas. La inhibición de la vía de RANKL, utilizando una droga que ya está en uso para el tratamiento de la osteoporosis y con muy pocos efectos secundarios, es altamente eficaz para evitar la aparición del cáncer de mama. Por supuesto, este tratamiento preventivo, tiene sentido para mujeres con alto riesgo de desarrollar un cáncer de mama, por ejemplo, mujeres con historia de cáncer familiar (portadoras de mutaciones en BRCA1 o BRCA2). Con un par de tratamientos anuales con este medicamento para la osteoporosis estas mujeres podrían evitar la mastectomía, que es la única solución preventiva actual.
¿Qué puede implicar esto para las pacientes de cáncer de mama?
El escenario de tratamiento una vez aparece el cáncer de mama es más complejo. El cáncer de mama es una enfermedad muy compleja y heterogénea, según la expresión de receptores hormonales, proteínas como HER2 y el hecho de que aparezca antes o después de la menopausia. Los resultados que tenemos hasta el momento en modelos de ratón indican que la inhibición de la vía puede disminuir la división celular e inducir muerte en algunos tumores de mama, pero no en todos. Por otro lado, estudios clínicos y preclínicos recientes demuestran que la inhibición de la vía reactiva la respuesta inmune anti-tumoral, potenciando el efecto de la inmunoterapia.
En el laboratorio tenemos en marcha estudios preclínicos con tumores de cáncer de mama procedentes de pacientes y también ensayos clínicos, con el objeto de identificar biomarcadores que nos permitan seleccionar a las mujeres con cáncer de mama, que podrían beneficiarse de este medicamento.
Has conseguido uno de los prestigiosos proyectos de investigación ERC Consolidator Grant, ¿crees que son escasas las ayudas de este tipo?
Sin duda, la financiación de la investigación básica es muy deficiente, y no solo en España (que ronda el 1,25% PIB), también en Europa (alrededor del 2% PIB de media). La mayor parte de la financiación europea de investigación está destinada a consorcios e investigación aplicada/traslacional. Pero el rédito de la investigación se fundamenta en la investigación básica que está claramente descuidada.
En estos tiempos de pandemia la sociedad se ha quedado con la impresión de que en menos de un año se pueden obtener vacunas, pero eso ha sido posible en base al conocimiento adquirido tras muchos años de investigación básica, que han llevado al descubrimiento del ADN, ARN, virus de ARN, respuesta inmune…
El programa ERC es una honrosa excepción que financia la investigación básica. A pesar del gran éxito de los investigadores españoles en las convocatorias ERC, son solo un porcentaje muy minoritario del total de investigadores que trabajan en España. Las ayudas ERC Starting y Consolidator son puntuales, destinadas a acelerar la investigación en los primeros años de tu carrera, para consolidarte en el campo, y optar luego a financiación de alto nivel en tu país. El problema en España es que esa financiación de alto nivel no existe, los proyectos nacionales conceden importes 10 veces más bajos que los proyectos ERC.
El cáncer de mama es uno en los que se ha logrado reducir más la mortalidad en las últimas décadas. ¿Qué avances crees que pueden ocurrir en los próximos años?
Efectivamente, los avances en cáncer de mama se han conseguido gracias a la mayor inversión (relativa) que se ha hecho en este tumor en comparación con otros cánceres. Es un ejemplo directo de que un aumento en la investigación (gracias a una mayor inversión), supone una mejora en la supervivencia. Creo que en los próximos años al entender mejor la heterogeneidad de la enfermedad, aumentará aún más la supervivencia, por la aparición de nuevas terapias dirigidas, y una mejor selección de los pacientes que los reciben. Confío en que mejore la respuesta a la inmunoterapia (con descubrimientos como el nuestro que propone usar Denosumab para mejorar la respuesta), y los tratamientos preventivos.
¿Cuándo pueden llegar nuevas terapias que estáis investigando a estas pacientes de cáncer de mama?
Algunas de las terapias ya han llegado, el problema es que, si no se seleccionan bien los pacientes, o las pautas de tratamiento, o las combinaciones de fármacos, algunas de estas terapias que podrían ser muy beneficiosas para un grupo de pacientes, terminan descartándose.
Hay que mejorar la racionalidad en el diseño de los ensayos clínicos y las terapias combinadas y aumentar los estudios ventana que permitan identificar biomarcadores de respuesta.
PERFIL
Sarah Teichmann
 Sarah Teichmann /A.Garrido. CNIO
Sarah Teichmann /A.Garrido. CNIO
Cuando fue elegida miembro de la Academia de Ciencias Médicas del Reino Unido, en 2015, sus colegas definieron a Sarah Teichmann como “la representante de una nueva estirpe de científicos en la interfaz entre la biología computacional y la biología molecular experimental”.
Teichmann (Karlsruhe, Alemania, 1975) es bióloga computacional. Lidera el Atlas de las Células Humanas, una colaboración de casi 300 laboratorios de todo el mundo para mapear las decenas de trillones de células, de cientos de clases diferentes, que constituyen el cuerpo humano.
Sus investigaciones se centran en estudiar los principios globales de las interacciones proteicas y la expresión génica. Sarah Teichmann dirige el programa de Genética Celular en el Wellcome Trust Sanger Institute, en Cambridge, Reino Unido, y es jefa de grupo en el Instituto Europeo de Bioinformática. Trabaja codo con codo con biólogos, programadores, físicos y matemáticos.
Sarah hizo su doctorado en el Laboratorio de Biología Molecular del MRC, en Cambridge, Reino Unido, y fue becaria en el Beit Memorial del University College de Londres. Inició un grupo en el Laboratorio de Biología Molecular del MRC en 2001. En 2013, se trasladó al Wellcome Genome Campus en Hinxton, Cambridge, donde su grupo está formado por investigadores del EMBL-Instituto Europeo de Bioinformática y del Wellcome Sanger Institute.
Es miembro de la Organización Europea de Biología Molecular (EMBO) y de la Academia de Ciencias Médicas, y su trabajo ha sido reconocido con varios premios, como el Premio Lister, la Medalla Colworth de la Sociedad Bioquímica, la Royal Society Crick Lecture y, en 2015, la Gold Medal de la EMBO.
Seminarios Distinguidos
07.05.2021
Agata Smogorzewska
The Rockefeller University (Estados Unidos)
'Tumorigenesis in the setting of DNA interstrand crosslink repair deficiency'
21.05.2021
Sara Buhrlage
Dana-Farber Cancer Institute (Estados Unidos)
'Integrated platform for DUB inhibitor discovery'
04.06.2021
Pascale Cossart
Instituto Pasteur (Francia)
'Infection biology in the era of microbiomes: the Listeria paradigm'
11.06.2021
Asifa Akhtar
Max Planck Institute of Immunobiology and Epigenetics (Alemania)
'X chromosome: A paradigm to study epigenetic regulation'
18.06.2021
Nuria Sebastián
Universidad Pompeu Fabra
'Languages before language: Infants’ early steps to learn language(s)'
Eventos WISE
24.06.2021
Marta Sanz
Escritora y filóloga
'La escritura: un viaje por el cuerpo humano' [vídeo]
