Esta web utiliza cookies para que podamos ofrecerte la mejor experiencia de usuario posible. La información de las cookies se almacena en tu navegador y realiza funciones tales como reconocerte cuando vuelves a nuestra web o ayudar a nuestro equipo a comprender qué secciones de la web encuentras más interesantes y útiles.
Columna
Estimados/as Amigos/as,
Espero que tanto vosotros como vuestras familias estéis bien.
En estos momentos tan preocupantes, me alegra mucho compartir con vosotros/as una buena noticia sobre el CNIO: acabamos de renovar la acreditación como Centro de Excelencia ‘Severo Ochoa’. Es la tercera vez consecutiva que el CNIO obtiene esta prestigiosa acreditación.
El programa Severo Ochoa es una herramienta del Gobierno de España para aumentar el nivel de excelencia en la investigación e innovación de nuestro país, gracias a que dota a los centros con financiación estable y flexible durante 5 años para poder llevar a cabo planes estratégicos. Es un programa ambicioso que permite que los centros de investigación españoles demuestren su potencial y compitan con los mejores del mundo. En el caso del CNIO, nos permitirá impulsar la biología computacional del cáncer en el Centro.
La pandemia que estamos viviendo nos recuerda que el bienestar de la sociedad pasa por la investigación biomédica: tanto la más básica, la que busca comprender por qué y cómo se producen las enfermedades, como la más orientada al paciente. Así lo hacemos en nuestro Centro, donde no solo producimos ciencia de vanguardia sino que somos capaces de convertirla en nuevas estrategias innovadoras, atrayendo el interés y la colaboración de la industria farmacéutica internacional.
Seguiremos honrando la acreditación de excelencia, que tenemos desde 2012, con nuestro trabajo incansable por los/as pacientes de cáncer. Y desde aquí felicito a nuestros/as investigadores/as, sin cuya labor y compromiso no habría sido posible este logro.
Maria Blasco
Directora
Noticias científicas CNIO
 Cuerpo embrionario de ratón con múltiples tipos celulares (marcados en diferentes colores) generado en cultivo después de la expresión de miR-203 en células madre. /CNIO
Cuerpo embrionario de ratón con múltiples tipos celulares (marcados en diferentes colores) generado en cultivo después de la expresión de miR-203 en células madre. /CNIO
Un equipo de nuestro Grupo de División Celular y Cáncer, que lidera Marcos Malumbres, ha descubierto una nueva tecnología, sencilla y rápida, para impulsar el potencial que tienen las células madre para especializarse en células adultas. Estas células se han convertido en una gran esperanza para la medicina regenerativa, pero una de sus principales limitaciones es su calidad. Ahora, gracias al método diseñado por el CNIO se podrá mejorar su calidad para que puedan ser empleadas en medicina regenerativa para afecciones musculares o alteraciones del sistema nervioso.
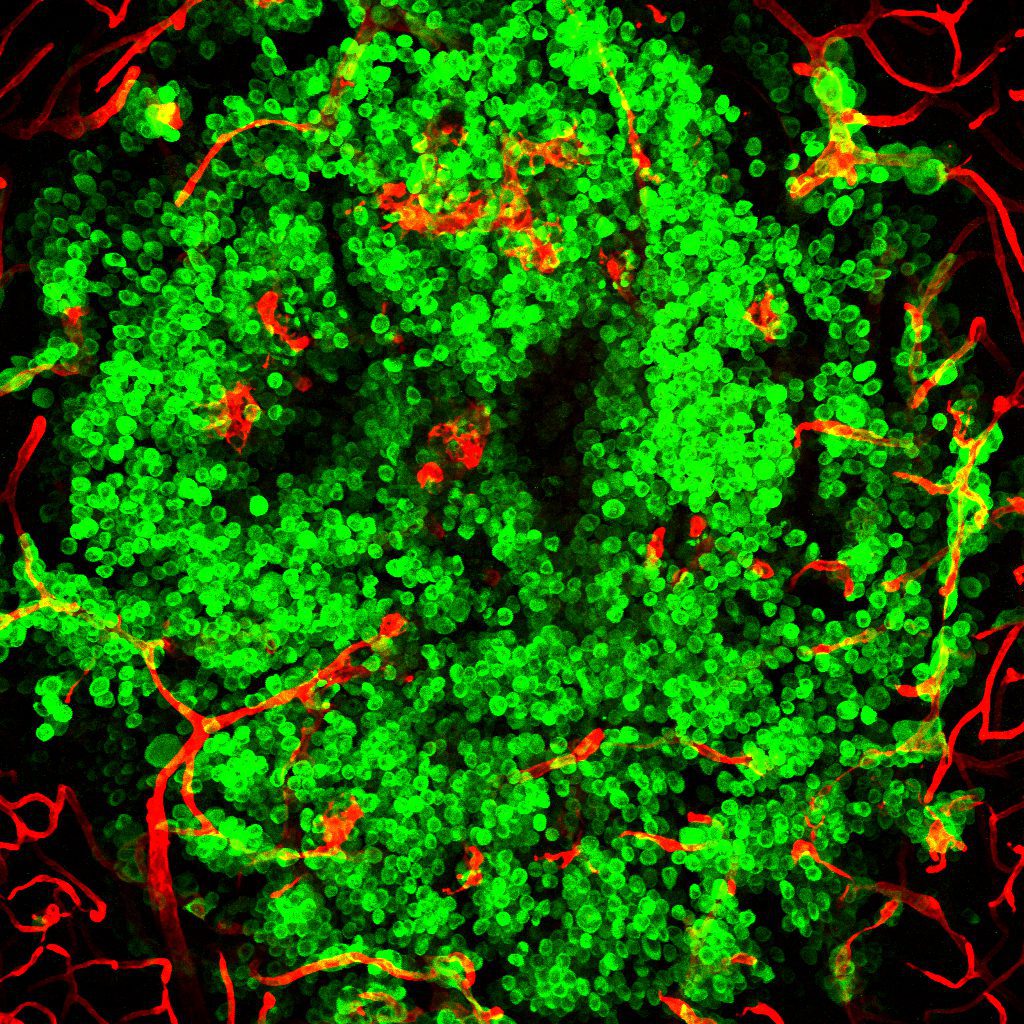 Células tumorales (en verde) invadiendo un cerebro de ratón, con los vasos sanguíneos en color rojo. /CNIO
Células tumorales (en verde) invadiendo un cerebro de ratón, con los vasos sanguíneos en color rojo. /CNIO
Las metástasis cerebrales (la aparición de tumores en el cerebro como consecuencia de un tumor en otro órgano) son uno de los grandes retos de la investigación del cáncer. Ahora, Manuel Valiente, jefe del Grupo de Metástasis Cerebral del CNIO, ha coordinado BrMPanel, el primer repositorio de líneas celulares para metástasis a cerebro, para “poner a disposición de otros grupos todo lo que sabemos y evitar la duplicación de trabajos que ya están hechos”.
Esperamos que esta base de datos ayudará a agilizar su estudio y a que más equipos científicos se animen a profundizar en esta área tan estratégica de la investigación del cáncer.
 Células de glioma (en azul) bajo tratamiento con temozolomida, con daño en el ADN marcado en color marrón. Cuando el locus de MGMT está intacto, su expresión se silencia y la temozolomida promueve el daño del ADN en todas las células tumorales (izquierda); Cuando se reorganiza el locus de MGMT, las células de glioma sobreexpresan MGMT, pueden reparar el daño y seguir creciendo (derecha). /CNIO
Células de glioma (en azul) bajo tratamiento con temozolomida, con daño en el ADN marcado en color marrón. Cuando el locus de MGMT está intacto, su expresión se silencia y la temozolomida promueve el daño del ADN en todas las células tumorales (izquierda); Cuando se reorganiza el locus de MGMT, las células de glioma sobreexpresan MGMT, pueden reparar el daño y seguir creciendo (derecha). /CNIO
Un equipo internacional liderado por Massimo Squatrito, del Grupo de Tumores Cerebrales Fundación Seve Ballesteros, ha descubierto las causas moleculares que hacen que algunos gliomas desarrollen resistencia al fármaco de quimioterapia temozolomida. Este hallazgo es fundamental para mejorar los métodos con los que se monitoriza la eficacia de esta terapia.
Además, en el futuro podría convertirse en una herramienta para detectar la aparición de la resistencia lo antes posible: “Mediante un sencillo análisis de biopsia líquida con solo unas muestras de sangre, podríamos saber qué pacientes están desarrollando resistencia a la temozolomida y ayudará a cambiar a otras opciones terapéuticas, cuando estén disponibles”.
En este boletín encontraréis una entrevista con Massimo Squatrito sobre su hallazgo.
 Desarrollo de los estadios iniciales de fibrosis pulmonar asociada al envejecimiento en ratones sin tratar (izqda.), que se previene en ratones tratados con la terapia génica en telomerasa (dcha.). /CNIO
Desarrollo de los estadios iniciales de fibrosis pulmonar asociada al envejecimiento en ratones sin tratar (izqda.), que se previene en ratones tratados con la terapia génica en telomerasa (dcha.). /CNIO
Investigadores del Grupo de Telómeros y Telomerasa, que dirige Maria Blasco, hacen un avance importante hacia una futura terapia génica contra la fibrosis pulmonar asociada al envejecimiento. “Nuestro resultado apunta a la posibilidad de crear una terapia capaz de prevenir el desarrollo de la fibrosis pulmonar asociada al envejecimiento en cualquier paciente”, afirma Blasco, directora del estudio.
El trabajo ha sido realizado en colaboración con la Universidad Complutense y la Universidad Autónoma de Barcelona.
 Secciones transversales de embriones murinos normales (WT) o sin STAG2 (KO) a día 9,5 de gestación teñidas con anticuerpos contra STAG2 (arriba) o hematoxilina-eosina (H-E, abajo) muestran el menor tamaño y una morfología anómala del corazón en ausencia de la cohesina STAG2. /CNIO
Secciones transversales de embriones murinos normales (WT) o sin STAG2 (KO) a día 9,5 de gestación teñidas con anticuerpos contra STAG2 (arriba) o hematoxilina-eosina (H-E, abajo) muestran el menor tamaño y una morfología anómala del corazón en ausencia de la cohesina STAG2. /CNIO
El tratamiento de enfermedades avanza sumando descubrimientos de lo más diversos. El CNIO y el CNIC acaban de dar un paso más, esclareciendo por qué la proteína que ‘abraza’ los cromosomas es clave en el cáncer y el desarrollo del corazón.
En 1998, Ana Losada, actualmente jefa del Grupo de Dinámica Cromosómica del CNIO, descubrió en vertebrados la cohesina, una proteína fundamental para la división de la célula. Hoy se sabe que también interviene en el cáncer, e investigadores en todo el mundo estudian por qué. Junto a Paco Real desde el CNIO y Miguel Manzanares desde el CNIC (actualmente en el CBMSO), han descubierto nuevas evidencias de que su mal funcionamiento contribuye a la enfermedad.
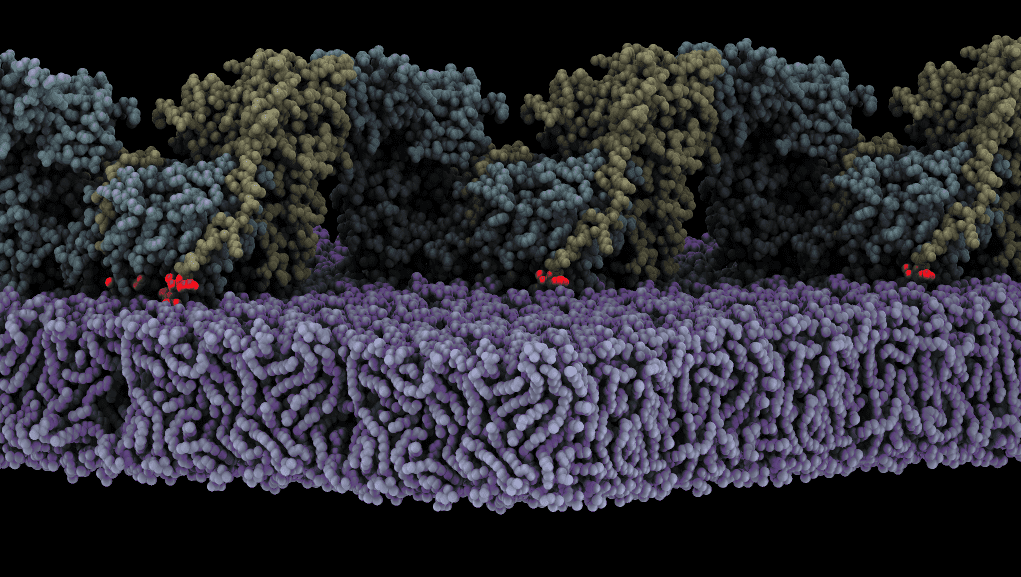 El ensamblaje de la forma oligomérica de FAK (amarillo/cian) en la membrana (morado) desencadena la autofosforilación. Se muestra un estado en el que el sitio de autofosforilación (rojo) está unido al sitio activo de la quinasa FAK. /CIB-CSIC
El ensamblaje de la forma oligomérica de FAK (amarillo/cian) en la membrana (morado) desencadena la autofosforilación. Se muestra un estado en el que el sitio de autofosforilación (rojo) está unido al sitio activo de la quinasa FAK. /CIB-CSIC
Un equipo de investigación dirigido por Daniel Lietha acaba de publicar los detalles del mecanismo de activación de la quinasa de adhesión focal (FAK) en las membranas lipídicas. Este mecanismo es clave para la invasión de células cancerosas promovida por la proteína FAK. Lietha inició esta investigación en el CNIO y la ha culminado en su actual institución, el Centro de Investigaciones Biológicas Margarita Salas (CIB-CSIC).
Nuestro Centro
 Imagen: A. Garrido. CNIO
Imagen: A. Garrido. CNIO
Grandes noticias: El CNIO recibe por tercera vez consecutiva la acreditación como Centro de Excelencia Severo Ochoa. Sin duda, un logro conjunto de todos/as nuestros/as investigadores/as, qu reafirma la importante contribución internacional del CNIO en comprender las bases moleculares del cáncer y abrir nuevas vías para la prevención, diagnóstico y tratamiento.
El comité evaluador ha valorado muy positivamente nuestras instalaciones punteras, nuestra avanzada posición en los rankings internacionales, un plan estratégico innovador, la complementariedad entre las áreas de investigación básica y clínica, la producción científica de nuestros/as investigadores/as en revistas internacionales de alto impacto, nuestras colaboraciones internacionales, nuestra estrategia transferencia tecnológica, nuestro plan de igualdad o la formación de jóvenes investigadores/as, entre otros.
 Óscar Fernández-Capetillo. /CNIO
Óscar Fernández-Capetillo. /CNIO
Y más buenas noticias: el Grupo de Inestabilidad Genómica, que dirige Óscar Fernández-Capetillo, ha recibido una financiación ERC Proof of Concept que concede el Consejo Europeo de Investigación para llevar a cabo un studio de inhibidores SETD8 durante un periodo de 18 meses. La financiación les permitirá avanzar en el desarrollo de estos compuestos que podrían ayudar a tratar tumores pediátricos de mal pronóstico.
“Por un lado intentaremos mejorar las propiedades de estos inhibidores y exploraremos su potencial antitumoral en modelos de ratón”, explica. Y por otro, lo más importante: “Trataremos de definir cuáles son las mutaciones específicas que confieren sensibilidad a este tratamiento, un área muy importante del desarrollo de fármacos ya que es necesaria para definir qué pacientes se beneficiarían de estos tratamientos”.
 Maria Blasco. /A. Garrido. CNIO
Maria Blasco. /A. Garrido. CNIO
Maria Blasco acaba de ser nombrada patrona del Museo Nacional del Prado. “Es un error pensar que la ciencia no está en las humanidades”, explica en esta entrevista para Servimedia.
Afirma que “siempre he sido una enamorada y admiradora del Museo del Prado, que creo que es uno de los museos más inspiradores y con más personalidad del mundo, y una de las instituciones más internacionales de nuestro país. Siempre ha sido una parada obligatoria cuando han venido amigos y colegas de todo el mundo y desde hace muchos años soy Amiga del Museo de Prado. Artistas y científicos/as compartimos la inquietud por el mundo y una mirada curiosa, que nos hace adentrarnos en lo desconocido”.
Entrevista
Massimo Squatrito: «En el futuro, podríamos detectar con un análisis de sangre qué pacientes de glioblastoma están desarrollando resistencia a la terapia»
 Massimo Squatrito. /A. Garrido. CNIO
Massimo Squatrito. /A. Garrido. CNIO
Hablamos con Massimo Squatrito, jefe de nuestro Grupo de Tumores Cerebrales Fundación Seve Ballesteros, sobre su último descubrimiento en glioblastomas, la forma más frecuente y agresiva de los tumores cerebrales primarios conocidos con el nombre de gliomas.
¿Cómo mejoran la supervivencia de los pacientes los actuales tratamientos para los glioblastomas?
Las modalidades de tratamiento para pacientes con gliomas malignos incluyen cirugía, radioterapia y quimioterapia. La cirugía suele ser el primer paso en el tratamiento de la mayoría de los tumores cerebrales. A menudo es el tratamiento ideal cuando se puede extirpar un tumor con un riesgo mínimo de daño neurológico. Luego, la radioterapia y la quimioterapia se utilizan para matar o ralentizar la proliferación de las células tumorales restantes.
Hace casi 15 años, el compuesto temozolomida se introdujo en la clínica como el principal enfoque quimioterapéutico para los gliomas malignos. Actualmente, es el único fármaco contra el cáncer para el que ensayos clínicos han demostrado que mejora la supervivencia en glioblastoma en un 30% cuando se administra con radioterapia.
Algunos pacientes desarrollan resistencia a este tratamiento. ¿Podrías hablarnos de vuestros descubrimientos sobre las bases moleculares de esta resistencia?
Desafortunadamente, no todos los pacientes con glioblastoma se benefician por igual del tratamiento con temozolomida: se ha demostrado que la población de pacientes que tiene la expresión más baja de una proteína llamada MGMT responde mejor a este compuesto, mientras que, por el contrario, los pacientes con niveles elevados de MGMT no responden tan bien al tratamiento. MGMT es una molécula clave que utilizan las células para reparar el daño inducido por la temozolomida.
En nuestro estudio hemos observado que un subconjunto de pacientes, que respondieron inicialmente a ella, adquirieron resistencia al fármaco durante el tratamiento al estimular la expresión de MGMT. Dicha activación de MGMT se logró poniendo su gen bajo el control de otros elementos genéticos, proceso que se conoce como ‘translocación de genes’ o ‘fusión de genes’. En nuestro laboratorio hemos podido recrear algunas de estas fusiones y hemos demostrado que, efectivamente, eran capaces de inducir resistencia a la temozolomida, tanto en células como en modelos animales.
¿Cómo beneficiarán a los pacientes estos hallazgos?
Un logro interesante de nuestro estudio fue detectar las fusiones del gen MGMT en la sangre de los modelos animales que desarrollaron esta resistencia. Si este hallazgo se confirma en pacientes con glioblastoma, en el futuro podría ser posible buscar la presencia de la fusión del gen MGMT en sangre para identificar a los pacientes que desarrollarán resistencia al tratamiento. La detección temprana de las fusiones de genes podría indicarnos cuándo los pacientes están desarrollando resistencia a la temozolomida, y se les podría recomendar que cambien a otras opciones terapéuticas cuando estén disponibles.
